Дистанційне навчання під час карантину
21.04.2020
17.04.2020
14.04.2020
10.04.2020
Тема. Контрольна
робота з теми «Неорганічні речовини та їхні
властивості»
Завдання:
Виконати контрольну роботу по варіантах.
І варіант
І рівень
1.Який ряд формул утворений лише з формул солей?
а) Na2S, MgCl2 , Ca3(PO4)3;
б) NaH, MgO, HPO3.
2. У яких виразах йдеться про кисень як просту речовину?
а)Оксиген входить до складу води;
б)у промисловості кисень добувають з повітря;в)газуватий кисень зберігають і перевозять у міцних сталевих балонах під тиском 150 ат.
3. Вкажіть порядковий номер елемента, атом якого має на зовнішньому рівні 3 електрони: а) 20; б) 21; в) 31.
4.Вкажіть рівняння реакції сполучення:
а)2А1(ОН)3 + 3Н2S04 -> А12(S04)3 + 6Н20;
б)2Na + 2Н20 -> 2NаОН + Н2;
в)2Fе + ЗВг2 = 2FеВг3
II рівень
5.Напишіть рівняння реакцій за наведеними схемами:
а) Н2 + N2
->….. ;
б)
СиО + Н2S04->….. .
6.Напишіть рівняння реакцій, за допомогою яких можна здійснити перетворення:
магній —» магній оксид —> магній карбонат —» карбон (IV) оксид —» кальцій карбонат.
7. Скільки з перелічених речовин можуть реагувати з хлоридною кислотою: натрій сульфат, барій оксид, цинк? а) одна; б)дві; в)три.
Напишіть рівняння відповідних реакцій та вкажіть їх типи.
III рівень
8.Напишіть не менше ніж чотири відмінних рівняння реакцій, що відбуваються з утворенням натрій гідроксиду.
9.Знайдіть масу солі, яка утвориться у результаті пропускання карбон (IV) оксиду масою 0,88 г крізь розчин масою 10 г з масовою часткою натрій гідроксиду 20%.
*10.Написати рівняння хімічних реакцій, що відбуваються в разі таких перетворень:
Al → Al2(SO4)3 → Al(OH)3 → Al2O3 ↓ ↓
AlCl3 NaAlO2 Зазначити типи хімічних реакцій, назвати зазначені речовини.
ІІ варіант
І рівень
1.До якого ряду хімічних формул не увійшли формули основ?
а) Сu(ОН)2, КОН, NH4ОН; б) HNO3, Nа2S04, МgН2.
2.Скільки нейтронів міститься у ядрі атома РЬ ?
а) 125; б) 4; в) 6.
3.Вкажіть рівняння реакцій обміну:
а)Н3Р04 + 2NаОН = Nа2НР04 + 2Н20;
б)FеС13 + 3КОН -> Fе(ОН)3 + 3KСІ;
в)Р205 + 3Н20 = 2Н3Р04.
4. У яких випадках мають на увазі хімічний елемент?
а)фосфор отруйний, опіки від нього дуже болючі;
б)фосфор у воді не розчиняється;
в)без фосфору немає життя;
г)білий фосфор має запах часнику.
ІІ рівень
5.Напишіть рівняння реакцій за наведеними схемами:
а) Ва + Н20->…..;
б) РЬ(NO3)2 + Н2S->…..
Яке з них є окисно-відновним? Відповідь мотивуйте рівнянням електронного балансу.
6.Напишіть рівняння реакцій, за допомогою яких можна здійснити перетворення: Цинк хлорид —> цинк гідроксид —> цинк оксид —> цинк сульфат —> цинк гідроксид.
7. Скільки з перелічених речовин можуть реагувати з кальцій оксидом: вода, купрум (II) оксид, карбон (IV) оксид? a) одна; б) дві; в)три.
Напишіть рівняння відповідних реакцій та вкажіть їх типи.
ІІІ рівень
8.Напишіть не менше ніж чотири принципово відмінних рівняння реакцій, що відбуваються з утворенням сульфур (IV) оксиду.
9.Обчисліть масу солі, яка утвориться у результаті пропускання 2,24 л вуглекислого газу (н. у.) крізь 25 г розчину з масовою часткою натрій гідроксиду 16%.
10*Написати рівняння хімічних реакцій, що відбуваються в разі таких перетворень:
Mg → MgO → Mg(NO3)2
↓
MgCl2
Зазначити типи хімічних реакцій, назвати зазначені речовини.
17.04.2020
Тема.
Узагальнення та систематизація знань з теми «Неорганічні речовини та їхні
властивості»
1.Виконати тести 20-35 с.187.
2.Здійснити схему перетворень з.36 с. 189
3.*Розв'язати задачу 42 с. 189.
14.04.2020
Тема. Виконання тренувальних вправ та розв'язок розрахункових задач
Завдання:
Виконати тести-онлайн і розв'язати задачі за
посиланням https://naurok.com.ua/test/rozv-yazuvannya-zadach-1-212162.html
10.04.2020
Тема. Виконання тренувальних вправ та розв'язок
розрахункових задач
Виконати завдання:
1. Вкажіть формулу вищого оксиду для хімічного
елемента з протонним числом 14: а) RO2 б) R2O в) R2O5
2.Здійсніть схему перетворень:
ZnS → SO2 → Na2SO3
↓
SO3 → H2SO4 → BaSO4 (5)
3.Реакцію 5 запишіть у йонно-молекулярній формі.
4.З водню
масою 60 г і відповідної
кількості азоту синтезували амоніак масою 272 г. Яка масова частка виходу
амоніаку по відношенню до теоретичного?
5. Обчисліть
масу вуглекислого газу, який можна добути у результаті взаємодії карбонату
кальцію масою 7 г з хлоридною кислотою масою 30 г, у якій масова
частка НСІ становить 20%.
6. Виберіть
сполуку, в якій Сульфур проявляє найнижчий ступінь окиснення:
а) Н2SO4; б)SO3; в) SO2; г) Н2S.
7. Розставте
коефіцієнти в рівнянні реакції методом електронного балансу, вкажіть окисник і
відновник: Мn + Н2SО4 = МnSО4 + S +
Н2O
8. Назвіть
солі за їхніми формулами: Mg3(PO4)2, NaHSO4, FeCl3, K2HPO4, NH4NO3, (NH4)2SO4, NaHCO3, MgHPO4, K2SiO3, Na2CO3.
9. Хром(ІІІ)
оксид масою 76 кг відновили методом алюмінотермії. Маса утвореного хрому становила 48 кг. Обчисліть відносний вихід продукту
реакції.
10. *Масові
частки калій, кальцій та силіцій(ІV) оксидів становлять відповідно 18,43 %,
10,98 % і 70,59 %. Установіть і запишіть формулу скла. Назвіть його .
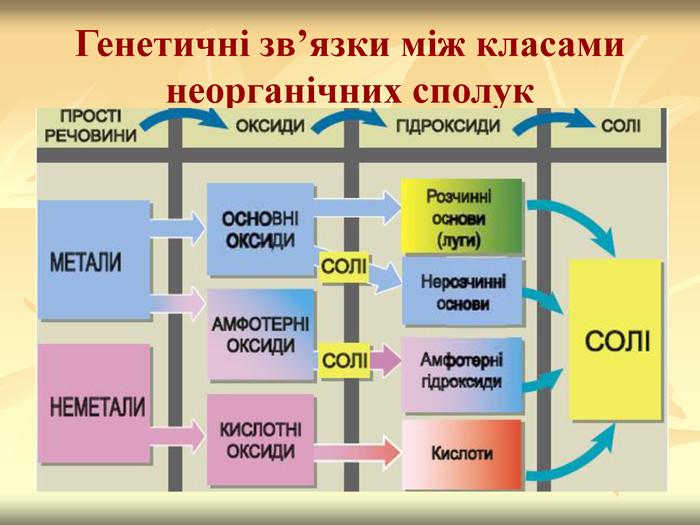
Тема.
Генетичні зв'язки між основними класами неорганічних і органічних сполук
Завдання:
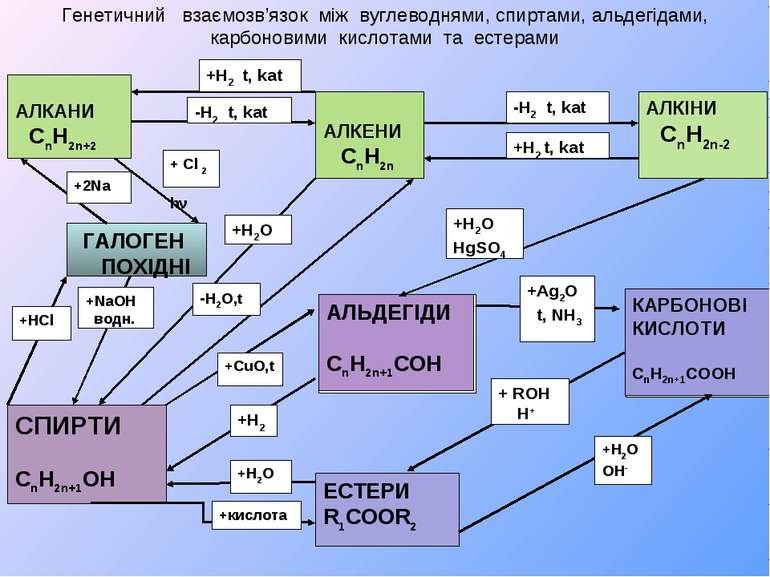
1.Переглянути відеопрезентацію «Генетичні зв'язки між класами
органічних сполук»за посиланням: https://www.youtube.com/watch?v=aIBWdpI-OfA
2. Cкладіть декілька схем генетичних зв’язків між зазначеними
речовинами й напишіть відповідні рівняння реакцій:
Ферум (ІІ) оксид, ферум(ІІІ) хлорид,
ферум(ІІ) гідроксид, ферум(ІІ) нітрат, залізо, ферум(ІІІ) оксид, ферум(ІІІ) сульфат, ферум(ІІІ) гідроксид.
03.04.2020
Тема. Генетичні зв’язки між основними класами неорганічних і
органічних сполук
Повторити § 34
Переглянути
схеми генетичного зв’язку.
Записати
рівняння реакції.
*Скласти
власний приклад генетичного зв’язку між основними класами неорганічних і органічних сполук

31.03.2020
Тема. Генетичні
зв’язки між основними класами неорганічних сполук
Завдання:
Повторити § 35
Переглянути відеоурок за посиланням: https://www.youtube.com/watch?v=t0q0n92QP7o
Тема.
Генетичні зв’язки між основними класами неорганічних сполук
Опрацювати § 34 підручника
Розгляньте схему генетичного зв’язку між основними класами неорганічних сполук.
Наприклад,
Завдання 1. Складіть рівняння реакцій відповідно до схеми:
Для реакцій 4, 5, 10, 11 — скласти окисно-відновні , реакції 6, 7, 8,
9 написати в йонно- молекулярній формі.
Завдання 2. З
перелічених речовин виберіть ті, з якими реагуватиме розчин сульфатної кислоти:
натрій гідроксид, купрум(II) оксид, золото, магній, барій хлорид, срібло,
алюміній гідроксид. Наведіть рівняння реакцій у молекулярній, повній та
скороченій йонній формах.
Завдання 3. Обчисліть
масу солі, що утворилася, якщо в реакцію вступило 34 г ферум(III) оксиду й 19,6
г сульфатної кислоти. (26,6 г)
Завдання 4. Обчисліть об’єм карбон(IV)
оксиду за н. у., що виділиться в результаті взаємодії 5,3 г натрій карбонату й
8 г сульфатної кислоти.
*Завдання 5. Обчисліть масу осаду, що
утвориться в результаті зливання 257 г розчину аргентум нітрату з масовою
часткою солі 3,4 % і 364 г розчину хлоридної кислоти з масовою часткою кислоти
2,92 %.
Завдання 1,2,5* с. 180 підручника
17.03.2020
Тема. Біологічне значення металічних та неметалічних елементів
Опрацювати §
32 підручника.
Виконати
завдання:
1 № 2,3,5 с.176
Завдання «Попрацюємо з медійними джерелами» с. 173.
Завдання
«Попрацюємо в групах» с.170.
Попрацюйте над навчальними проектами за темами (на вибір):
1.Неорганічні речовини у фармації (або в домашній аптечці) і харчовій промисловості.
2.Властивості і застосування карбонатів, нітратів і ортофосфатів лужних і лужноземельних металічних елементів, солей амонію.
Підготуйте презентацію за вибраною темою.


Немає коментарів:
Дописати коментар